Domande e casi di laboratorio “Lo scopo non è tanto vedere quello che nessuno ha ancora visto, quanto pensare quello che nessuno ha ancora pensato di quello che tutti vedono.”(Arthur Schopenhauer) “Non esistono malattie. Esistono solo malati.”(Armand Trousseau) Mentre ho riservato una pagina a parte alle domande sui contenuti e sul significato di questo sito, in questa pagina sono via via raccolte le risposte alle domande che inevitabilmente, si tratti di analisi tradizionali o di analisi genetiche, sorgono in merito alla interpretazione dei risultati delle analisi di laboratorio. Interpretare le analisi di laboratorio non sempre è banale, e non sempre è un processo immediato e lineare come si vorrebbe. Per cui può accadere che quello che sembra “intuitivamente evidente”, e magari in certe circostanze ha portato alla conclusione corretta, in altre circostanze porti a conclusioni sbagliate. Questo può per esempio accadere quando la conclusione dipende non tanto da una singola osservazione, per quanto questa possa apparire dotata di “evidente” forza esplicativa, quanto invece dal contesto in cui questa è calata. In questi casi le scorciatoie cognitive possono portare all’interpretazione sbagliata (per capire i presupposti di questa affermazione rimando alla parte del sito riservata agli errori cognitivi). Le domande e i casi che riporto sono discussi ispirandosi alla metodologia del case study e, attraverso lo studio e l’approfondimento di casi mirati, hanno lo scopo di favorire lo sviluppo di una interazione costruttiva tra il laboratorio, il paziente e il clinico che lo ha in cura. → Anticorpi anti-toxoplasma della classe IgG→ Il caso degli anticorpi contro il virus dell’epatite C (anticorpi anti-HCV)→ Le unità di misura della clearance delle creatinina→ eGFR (estimated Glomerular Filtration Rate)→ Test di laboratorio per l’influenza (di tipo A e di tipo B)→ Il caso dei trigliceridi Anticorpi anti toxoplasma della classe IgG Una paziente, gravida, ci segnala il fatto che presso il nostro laboratorio ha avuto un referto nel quale gli anticorpi anti-toxoplasma della classe IgG risultavano presenti, mentre in precedenza, in un altro laboratorio, gli anticorpi anti-toxoplasma della classe IgG risultavano assenti. E ci chiede se vi sia una spegazione del fatto, assunto che nessuno dei due laboratori ha commesso uno sbaglio, in quanto in entrambi i casi risultati sono stati confermati su differenti prelievi. Mentre per un inquadramento completo, concettuale e tecnico, del problema, rimando alla parte sul teorema di Bayes, e in particolare all'approfondimento contenuto nella parte su teorema di Bayes e strategie diagnostiche, cerco di riassumere qui brevemente la questione. Se si selezionano un primo gruppo di soggetti che non sono mai venuti in contatto con il toxoplasma (soggetti non immuni) e un secondo gruppo di soggetti che sono sicuramente guariti dall'infezione (soggetti immuni), e si determina la concentrazione delle IgG nel siero con un test diagnostico in grado di rilevare le IgG anti-toxoplasma, si ottengono due distribuzioni simili a quelle qui riportate 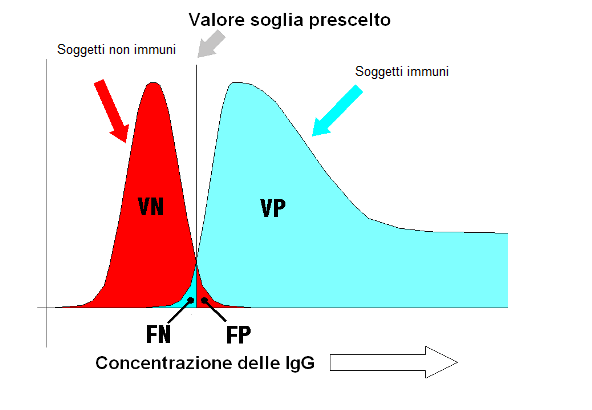 Una volta scelto un valore soglia per separare i soggetti di un gruppo da quelli dell'altro gruppo, si trova che la maggior parte dei soggetti del primo gruppo (non immuni) viene classificato correttamente dal test diagnostico (sono i veri negativi = VN), e che la maggior parte dei soggetti del secondo gruppo (soggetti immuni) viene classificata correttamente dal test diagnostico (sono i veri positivi = VP). Tuttavia, a causa dei limiti inerenti a qualsasi tipo di test/classificazione, accade anche che qualche soggetto senza le IgG sia classificato dal test come soggetto che le ha (FP = falsi positivi), e per converso accade che qualche soggetto con le IgG sia classificato come soggetto che non le ha (FN = falsi negativi). In un recente lavoro [Maudry A, Chene G, Chatelain R, Patural H, Bellete B, Tisseur B, Hafid J, Raberin H, Beretta S, Tran Manh Sung R, Belot G, Flori P. Bicentric Evaluation of Six Anti-Toxoplasma Immunoglobulin G (IgG) Automated Immunoassays and Comparison to the Toxo II IgG Western Blot. Clinical and vaccine imunology, Sept. 2009, p. 1322–1326] sono stati presi in considerazione i principali test diagnostici di routine per la determinazione nel siero degli anticorpi anti-toxoplasma della classe IgG, confrontandoli con un test (immunoblotting) di secondo livello, più complesso e più costoso, ma ritenuto anche più accurato. I test diagnostici di routine hanno dimostrato di avere sensibilità e specificità eccellenti, come illustrato nelle tabella che segue. Ma non sono in grado di fornire la certezza assoluta (che si avrebbe solamente nel caso di un test con una sensibilità uguale al 100% e una specificità uguale al 100%: valori irraggiungibili nella pratica).
Una volta scelto un valore soglia per separare i soggetti di un gruppo da quelli dell'altro gruppo, si trova che la maggior parte dei soggetti del primo gruppo (non immuni) viene classificato correttamente dal test diagnostico (sono i veri negativi = VN), e che la maggior parte dei soggetti del secondo gruppo (soggetti immuni) viene classificata correttamente dal test diagnostico (sono i veri positivi = VP). Tuttavia, a causa dei limiti inerenti a qualsasi tipo di test/classificazione, accade anche che qualche soggetto senza le IgG sia classificato dal test come soggetto che le ha (FP = falsi positivi), e per converso accade che qualche soggetto con le IgG sia classificato come soggetto che non le ha (FN = falsi negativi). In un recente lavoro [Maudry A, Chene G, Chatelain R, Patural H, Bellete B, Tisseur B, Hafid J, Raberin H, Beretta S, Tran Manh Sung R, Belot G, Flori P. Bicentric Evaluation of Six Anti-Toxoplasma Immunoglobulin G (IgG) Automated Immunoassays and Comparison to the Toxo II IgG Western Blot. Clinical and vaccine imunology, Sept. 2009, p. 1322–1326] sono stati presi in considerazione i principali test diagnostici di routine per la determinazione nel siero degli anticorpi anti-toxoplasma della classe IgG, confrontandoli con un test (immunoblotting) di secondo livello, più complesso e più costoso, ma ritenuto anche più accurato. I test diagnostici di routine hanno dimostrato di avere sensibilità e specificità eccellenti, come illustrato nelle tabella che segue. Ma non sono in grado di fornire la certezza assoluta (che si avrebbe solamente nel caso di un test con una sensibilità uguale al 100% e una specificità uguale al 100%: valori irraggiungibili nella pratica).
Come sempre accade, aumentando la sensibilità del test [ovvero diminuendo il valore soglia a partire dal quale si assume che le IgG siano presenti in concentrazioni che proteggono dalla reinfezione] aumentano i falsi positivi, mentre aumentando la specificità del test [ovvero aumentando il valore soglia a partire dal quale si assume che le IgG siano presenti in concentrazioni che proteggono dalla reinfezione] aumentano i falsi negativi. Nel caso della paziente, il test è stato effettuato in entrambi i casi con test validi dal punto di vista analitico: ma la prima volta in un laboratorio che utilizzava un metodo un poco più specifico, la seconda volta in un laboratorio che utilizzava un test un poco più sensibile. Ed ecco allora la domanda, semplice e concreta: ma la paziente ha o non ha le IgG anti-toxoplasma? In questo caso (fortunatamente si tratta di casi abbastanza rari) la sola possibilità di ripondere alla domanda è di effettuare un test di secondo livello, come l'immunoblotting, che è in grado di stabilire, con un grado di accuratezza molto elevato se la paziente ha o non ha le IgG anti-toxoplasma. Starà poi al clinico stabilire se magari, in base al principio di maggior cautela, nel caso specifico la paziente debba comunque adottare tutte le precauzioni previste per le pazienti gravide non immuni (precauzioni facilmente adottabili) anche qualora il test di secondo livello dovesse stabilire la presenza di IgG anti-toxoplasma. Il caso degli anticorpi contro il virus dell’epatite C (anticorpi anti-HCV) Un paziente chiede un chiarimento in quanto, di fronte ad un test con un risultato di anticorpi anti-HCV presenti, ha ripetuto lo stesso test in un altro laboratorio, ottenendo un risultato di anticorpi anti-HCV assenti. La possibilità che un test per la ricerca degli anticorpi anti-HCV (anticorpi contro il virus dell'epatite C) risulti positivo in un laboratorio e negativo in un altro laboratorio può in effetti lasciare sconcertati coloro che non hanno mai avuto l’occasione di affrontare il tema della sensibilità, della specificità e del valore predittivo di un test di laboratorio. Rimando come sempre, per la familiarizzazione con gli strumenti che ci consentono di misurare il valore aggiunto che un test di laboratorio è in grado di fornire al medico in termini di informazione diagnostica, al tema del sito cui sono più affezionato, quello concernente il teorema di Bayes nella diagnostica di laboratorio e alle numerose pagine in cui il tema è sviluppato. Il caso degli anticorpi anti-HCV ci consente di ricordare che nel caso di problemi diagnostici di una certa complessità l’approccio più razionale consiste nel procedere per gradi. Nella diagnostica dell’infezione da virus dell’epatite C il primo passo consiste nell’utilizzare un test di primo livello, un test indiretto che rileva la presenza nel siero di anticorpi contro il virus dell’epatite C (anticorpi anti-HCV). Si tratta di un test abbastanza semplice e relativamente poco costoso, per il quale è stato scelto un valore soglia tra sani e malati tale da conferire al test una sensibilità del 100% (il 100% dei malati viene individuato dal test) anche se questo comporta una specificità inferiore al 100%. Una sensibilità del 100% comporta un valore predittivo del test negativo del 100%, e l’assenza di falsi negativi (FN). I soggetti con il test negativo hanno una probabilità del 100% dei essere sani (sono veri negativi, VN), e possono pertanto essere esclusi dal successivo iter diagnostico. 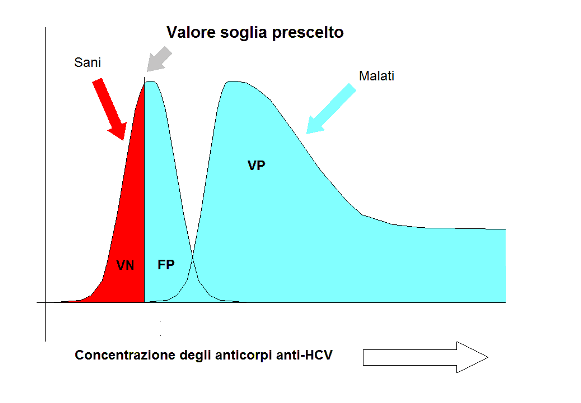 Una specificità inferiore al 100% comporta un valore predittivo del test positivo inferiore al 100%: questo significa che il test è positivo sia nei soggetti malati (nel caso specifico in tutti i soggetti malati, data la sensibilità del 100% del test) sia in alcuni soggetti sani. Sui soggetti risultati positivi al test di primo livello viene allora eseguito un test di secondo livello, più complesso e costoso, ma più specifico (per esempio un test diretto per la ricerca nel sangue dell’RNA del virus dell’epatite C). Il test di secondo livello consente di discriminare all’interno dei soggetti risultati positivi al test di primo livello i veri positivi (VP), cioè i soggetti con infezione da virus dell’epatite C, dai falsi positivi (FP), soggetti senza infezione ma nei quali il test di primo livello è risultato positivo: e non per un errore del laboratorio, ma semplicemente per i limiti intrinseci al test di primo livello, limiti derivanti dalla scelta di una soglia tra sani e malati che ha privilegiato la sensibilità, pagando per questo lo scotto sotto forma di una riduzione della specificità del test. Questo concetto lo trovate sviluppato nella parte dedicata a strategie diagnostiche e teorema di Bayes in particolare nel problema 7 della parte riservata agli esempi. Ho preparato una breve discussione sull'argomento anticorpi anti-HCV che risponde ai dubbi del paziente, e che mi pare utile e didattica. Le unità di misura della clearance della creatinina Un paziente ci ha chiesto un chiarimento in merito alle unità di misura nelle quali è espressa la clearance della creatinina. Rispondo con questo breve documento, dal titolo magari un pò ovvio, “Quali sono le unità di misura nelle quali espressa la clearance della creatinina?”, ma che consente di mettere a fuoco alcuni concetti della massima importanza, indispensabili anche per meglio comprendere le argomentazioni che stanno alla base del no alla presenza nel referto di laboratorio dell’eGFR, che gli (eventuali) interessati possono trovare al punto seguente. eGFR - Anatomia di una equazione Un paziente ci chiede se eseguiamo l’analisi denominata “eGFR”. Preciso subito che l’eGFR non è una analisi che viene eseguita “fisicamente” sul sangue del paziente. L’eGFR è il valore numerico che risulta dalla applicazione di una equazione matematica al risultato di un’altra analisi, questa invece comune e assai frequentemente eseguita: la determinazione della concentrazione della creatinina nel siero. Ma la domanda è molto, molto interessante. Premetto che come medico di laboratorio il mio dovere è contribuire ad estendere i sensi del medico/clinico con l’informazione derivante dallo studio dell’organismo in dimensioni che sfuggono all’osservazione diretta da parte del clinico nel suo rapporto con il paziente: fatto che rende significativa la piccolissima parte di medicina di mia competenza. Per fare questo mi sono sempre basato su metodo e principi della scienza: anche se scienza applicata, il laboratorio clinico è fatto di metodo e principi scientifici. E’ sulla base di questa idea fondamentale, sulla quale ho basato la mia vita professionale, che intervengo sul tema dell’eGFR, la “velocità di filtrazione glomerulare stimata”. L’argomento è complesso, tanto che ho dovuto svilupparlo in uno scritto a parte, che ho intitolato “eGFR (estimated Glomerular Filtration Rate) - Anatomia di una equazione. Ho quindi aggiunto un altro scritto, più conciso, semplificato dal punto di vista tecnico, e maggiormente orientato a illustrare le ragioni del no, dal titolo “’Dalla creatinina nel siero all’eGFR e ritorno. I perchè di un no alla presenza dell’eGFR nel referto di laboratorio”. Sono certo che entrambi aiuteranno il nostro paziente a comprendere perché, in attesa che la situazione si chiarisca dal punto di vista scientifico, nei referti del nostro laboratorio non compare l’eGFR. Test di laboratorio per l’influenza (di tipo A e di tipo B) Un paziente ci chiede per quale ragione abbiamo deciso di non eseguire nel nostro laboratorio il test per l’influenza (test per l’infezione da virus dell’influenza di tipo A [che include il virus definito come A(H1N1)v] e di tipo B). Innanzitutto va premesso che per la diagnosi di infezione da virus influenzali esistono vari tipi di test, ma che solamente un tipo di test, che fornisce una “ragionevole presunzione” di infezione, denominato “test rapido”, è alla portata dei comuni laboratori di analisi cliniche. I test che forniscono la “certezza” di infezione prevedono la coltura dei virus su cellule umane e, sia per la sicurezza degli operatori sia (e questa è la ragione principale) per la tutela della salute pubblica (per evitare fughe di virus con i potenziali danni conseguenti sulla popolazione), sono richieste condizioni operative così stringenti che (per esempio) in Italia solamente tre laboratori sono in grado di assicurare questi test, che chiamiamo “test di riferimento”. Dato che la tutela della salute pubblica è uno degli interessi principali dello Stato, tutti i governi (anche quelli che non hanno un sistema sanitario pubblico) hanno messo a disposizione dei cittadini informazioni assolutamente aggiornate in merito, e sul web potete trovare una quantità quasi illimitata di informazioni scientificamente corrette da fonti attendibili (si tratta solo di saperle selezionare). Ma la domanda è oltremodo interessante, perchè mi consente di appellarmi al contenuto del mio sito www.bayes.it che, tra premesse, formule, esempi e programmi, ho dedicato quasi per metà al teorema di Bayes. Che anche nel caso dell’influenza riveste un ruolo esplicativo centrale: vediamo come, partendo dalla citazione di due (tra i tanti) lavori che lo utilizzano/ne utilizzano i presupposti. Nel lavoro “C.K.Y. Cheng et al. / Factors affecting QuickVue Influenza A + B rapid test performance in the community setting / Diagnostic Microbiology and Infectious Disease 65 (2009) 35–41” si afferma che “i test rapidi hanno una sensibilità di 0.68 e una specificità di 0.96 quando confrontati con la coltura del virus”. Nel lavoro “C. Ruef / Diagnosing Influenza – Clinical Assessment and/or Rapid Antigen Testing? / Infection 2007; 35: 49–50” si afferma che la diagnosi di influenza basata sui segni clinici [insorgenza acuta, febbre elevata e tosse secca] ha una “sensibilità del 33% e specificità del 98%.” Sono queste due affermazioni sufficienti per trarre una qualche conclusione? Direi proprio di si. Guardate le due seguenti tabelle, ottenute mediante il mio semplicissimo programma per il calcolo del valore predittivo di un test di laboratorio a partire da sensibilità, specificità e prevalenza, utilizzando il teorema di Bayes. Impiegando i valori di sensibilità (0,68) e di specificità (0,96) dei test rapidi indicati da Cheng si ottengono, in funzione dei valori della prevalenza della malattia “influenza” che vanno dal 5 per mille (0,005) al 20% (0,20), il valore predittivo di un test positivo (VPT+) e il valore predittivo di un test negativo (VPT-) che trovate qui nelle due colonne di destra:
Una specificità inferiore al 100% comporta un valore predittivo del test positivo inferiore al 100%: questo significa che il test è positivo sia nei soggetti malati (nel caso specifico in tutti i soggetti malati, data la sensibilità del 100% del test) sia in alcuni soggetti sani. Sui soggetti risultati positivi al test di primo livello viene allora eseguito un test di secondo livello, più complesso e costoso, ma più specifico (per esempio un test diretto per la ricerca nel sangue dell’RNA del virus dell’epatite C). Il test di secondo livello consente di discriminare all’interno dei soggetti risultati positivi al test di primo livello i veri positivi (VP), cioè i soggetti con infezione da virus dell’epatite C, dai falsi positivi (FP), soggetti senza infezione ma nei quali il test di primo livello è risultato positivo: e non per un errore del laboratorio, ma semplicemente per i limiti intrinseci al test di primo livello, limiti derivanti dalla scelta di una soglia tra sani e malati che ha privilegiato la sensibilità, pagando per questo lo scotto sotto forma di una riduzione della specificità del test. Questo concetto lo trovate sviluppato nella parte dedicata a strategie diagnostiche e teorema di Bayes in particolare nel problema 7 della parte riservata agli esempi. Ho preparato una breve discussione sull'argomento anticorpi anti-HCV che risponde ai dubbi del paziente, e che mi pare utile e didattica. Le unità di misura della clearance della creatinina Un paziente ci ha chiesto un chiarimento in merito alle unità di misura nelle quali è espressa la clearance della creatinina. Rispondo con questo breve documento, dal titolo magari un pò ovvio, “Quali sono le unità di misura nelle quali espressa la clearance della creatinina?”, ma che consente di mettere a fuoco alcuni concetti della massima importanza, indispensabili anche per meglio comprendere le argomentazioni che stanno alla base del no alla presenza nel referto di laboratorio dell’eGFR, che gli (eventuali) interessati possono trovare al punto seguente. eGFR - Anatomia di una equazione Un paziente ci chiede se eseguiamo l’analisi denominata “eGFR”. Preciso subito che l’eGFR non è una analisi che viene eseguita “fisicamente” sul sangue del paziente. L’eGFR è il valore numerico che risulta dalla applicazione di una equazione matematica al risultato di un’altra analisi, questa invece comune e assai frequentemente eseguita: la determinazione della concentrazione della creatinina nel siero. Ma la domanda è molto, molto interessante. Premetto che come medico di laboratorio il mio dovere è contribuire ad estendere i sensi del medico/clinico con l’informazione derivante dallo studio dell’organismo in dimensioni che sfuggono all’osservazione diretta da parte del clinico nel suo rapporto con il paziente: fatto che rende significativa la piccolissima parte di medicina di mia competenza. Per fare questo mi sono sempre basato su metodo e principi della scienza: anche se scienza applicata, il laboratorio clinico è fatto di metodo e principi scientifici. E’ sulla base di questa idea fondamentale, sulla quale ho basato la mia vita professionale, che intervengo sul tema dell’eGFR, la “velocità di filtrazione glomerulare stimata”. L’argomento è complesso, tanto che ho dovuto svilupparlo in uno scritto a parte, che ho intitolato “eGFR (estimated Glomerular Filtration Rate) - Anatomia di una equazione. Ho quindi aggiunto un altro scritto, più conciso, semplificato dal punto di vista tecnico, e maggiormente orientato a illustrare le ragioni del no, dal titolo “’Dalla creatinina nel siero all’eGFR e ritorno. I perchè di un no alla presenza dell’eGFR nel referto di laboratorio”. Sono certo che entrambi aiuteranno il nostro paziente a comprendere perché, in attesa che la situazione si chiarisca dal punto di vista scientifico, nei referti del nostro laboratorio non compare l’eGFR. Test di laboratorio per l’influenza (di tipo A e di tipo B) Un paziente ci chiede per quale ragione abbiamo deciso di non eseguire nel nostro laboratorio il test per l’influenza (test per l’infezione da virus dell’influenza di tipo A [che include il virus definito come A(H1N1)v] e di tipo B). Innanzitutto va premesso che per la diagnosi di infezione da virus influenzali esistono vari tipi di test, ma che solamente un tipo di test, che fornisce una “ragionevole presunzione” di infezione, denominato “test rapido”, è alla portata dei comuni laboratori di analisi cliniche. I test che forniscono la “certezza” di infezione prevedono la coltura dei virus su cellule umane e, sia per la sicurezza degli operatori sia (e questa è la ragione principale) per la tutela della salute pubblica (per evitare fughe di virus con i potenziali danni conseguenti sulla popolazione), sono richieste condizioni operative così stringenti che (per esempio) in Italia solamente tre laboratori sono in grado di assicurare questi test, che chiamiamo “test di riferimento”. Dato che la tutela della salute pubblica è uno degli interessi principali dello Stato, tutti i governi (anche quelli che non hanno un sistema sanitario pubblico) hanno messo a disposizione dei cittadini informazioni assolutamente aggiornate in merito, e sul web potete trovare una quantità quasi illimitata di informazioni scientificamente corrette da fonti attendibili (si tratta solo di saperle selezionare). Ma la domanda è oltremodo interessante, perchè mi consente di appellarmi al contenuto del mio sito www.bayes.it che, tra premesse, formule, esempi e programmi, ho dedicato quasi per metà al teorema di Bayes. Che anche nel caso dell’influenza riveste un ruolo esplicativo centrale: vediamo come, partendo dalla citazione di due (tra i tanti) lavori che lo utilizzano/ne utilizzano i presupposti. Nel lavoro “C.K.Y. Cheng et al. / Factors affecting QuickVue Influenza A + B rapid test performance in the community setting / Diagnostic Microbiology and Infectious Disease 65 (2009) 35–41” si afferma che “i test rapidi hanno una sensibilità di 0.68 e una specificità di 0.96 quando confrontati con la coltura del virus”. Nel lavoro “C. Ruef / Diagnosing Influenza – Clinical Assessment and/or Rapid Antigen Testing? / Infection 2007; 35: 49–50” si afferma che la diagnosi di influenza basata sui segni clinici [insorgenza acuta, febbre elevata e tosse secca] ha una “sensibilità del 33% e specificità del 98%.” Sono queste due affermazioni sufficienti per trarre una qualche conclusione? Direi proprio di si. Guardate le due seguenti tabelle, ottenute mediante il mio semplicissimo programma per il calcolo del valore predittivo di un test di laboratorio a partire da sensibilità, specificità e prevalenza, utilizzando il teorema di Bayes. Impiegando i valori di sensibilità (0,68) e di specificità (0,96) dei test rapidi indicati da Cheng si ottengono, in funzione dei valori della prevalenza della malattia “influenza” che vanno dal 5 per mille (0,005) al 20% (0,20), il valore predittivo di un test positivo (VPT+) e il valore predittivo di un test negativo (VPT-) che trovate qui nelle due colonne di destra:
Impiegando i valori di sensibilità (0,33) e di specificità (0,98) dei segni clinici indicati da Ruef si ottengono, in funzione dei valori della prevalenza della malattia “influenza” che vanno dal 5 per mille (0,005) al 20% (0,20), il valore predittivo di un test positivo (VPT+) e il valore predittivo di un test negativo (VPT-) che trovate qui nelle due colonne di destra:
Il fatto notevole è che nel caso del test rapido per l’influenza (fortunatamente è uno dei rarissimi casi: se fosse sempre così come medico di laboratorio sarei già da tempo rimasto senza lavoro!) a parità di prevalenza della malattia il valore predittivo di un test di laboratorio positivo è sovrapponibile a quello della diagnosi clinica (basata sui segni: insorgenza acuta, febbre elevata e tosse secca). Per la precisione il valore predittivo di un test positivo (VPT+, la probabilità di essere ammalato per un soggetto con un test positivo) è perfettamente identico, mentre il valore predittivo di un test negativo (VPT-, la probabilità di essere sano per un soggetto con un test negativo) è, considerata l’incertezza della conclusione statistica, sostanzialmente analogo. Questo conferma la conclusione di Ruef nell’editoriale sopra citato che “…data la relativamente bassa sensibilità del test rapido e i dati limitati riguardanti la sua ricaduta sul trattamento del paziente … l’impiego generalizzato di questo test al momento non può essere raccomandato...”. Per questa ragione abbiamo deciso di non eseguire nel nostro laboratorio il test rapido per l’influenza (test per l’infezione da virus dell’influenza di tipo A [che include il virus definito come A(H1N1)v] e di tipo B). Il test potrà invece essere eventualmente eseguito presso lo stesso ambulatorio del medico curante al momento della visita (il test richiede solamente 10 minuti, non presenta alcuna difficoltà tecnica di esecuzione, e non richiede alcuna specifica capacità tecnica per l’interpretazione dei risultati) in presenza di una sintomatologia significativa, e a discrezione del medico e del paziente, al fine di integrare in casi specifici l’informazione derivante dalla diagnosi clinica.. Il caso dei trigliceridi Un paziente effettua una serie di analisi tra le quali è inclusa la determinazione di trigliceridi, che risultano avere una concentrazione di 1108 mg/dL. Dopo tre settimane ripete la determinazione dei trigliceridi, che risultano ora avere una concentrazione di 242 mg/dL. Il paziente decide di fare le proprie rimostranze, e sporge reclamo all’Ufficio Relazioni con il Pubblico, convinto che il laboratorio la prima volta abbia commesso uno sbaglio. L’analisi del problema evidenzia i seguenti punti:1) il laboratorio in questione è certificato UNI EN ISO 9001:2000, e questo garantisce il controllo del processo analitico in tutte le fasi;2) le provette sono identificate al momento del prelievo con un codice a barre, sono riconosciute automaticamente dallo strumento, che trasmette automaticamente il risultato al referto, escludendo quindi la possibilità di scambi di campione e/o di errori di trascrizione;3) i controlli di qualità nei due giorni in oggetto indicavano una situazione perfettamente sotto controllo;4) la strumentazione del laboratorio per valori dei trigliceridi superiori a 600 mg/dL ripete automaticamente l'analisi, cosa che è avvenuta nella prima delle due occasioni, e che ha confermato il risultato elevato riscontrato (i due risultati sono stati registrati nel log-file dello strumento);5) i valori desiderabili raccomandati per i lipidi nel siero sono definiti in condizioni standard, rappresentate da 12 ore di digiuno prima del prelievo, e pertanto è assolutamente necessario rispettare le 12 ore di digiuno prima del prelievo al fine di potere confrontare tra di loro risultati successivi. Un sovraccarico calorico la sera precedente l'esame può comportare elevazioni anche rilevanti della concentrazioni di questi analiti, (in particolar modo dei trigliceridi) se l'analisi viene effettuata prima di 12 ore dall'ultimo pasto: questo in quanto l'eccesso di calorie (ancor più rilevante se ai cibi viene associato il consumo di alcool, che ha un potere calorico molto elevato) viene fisiologicamente trasformato dall'organismo in trigliceridi, destinati ad essere depositati nel tessuto adiposo, e che rimangono in circolo a lungo prima di ritornare ai livelli tipici del soggetto;6) le “Linee Guida per la Diagnostica di Laboratorio delle Dislipidemie” della Società Italiana di Biochimica Clinica e di Biologia Molecolare Clinica, confermano il fatto che "...Variabilità preanalitica... i trigliceridi (TG) presentano una variabilità biologica intraindividuale molto elevata, maggiore di quella che è stata riscontrata per gli altri costituenti lipidici del plasma... Il ruolo giocato dalle variabili preanalitiche ed il controllo delle loro diverse cause assumono quindi un’importanza fondamentale nella standardizzazione dei procedimenti di misura dei TG per il controllo della variabilità preanalitica valgono le stesse considerazioni del colesterolo totale. Raccomandazioni particolari riguardano l’astensione dal fumo e dall’esercizio fisico, nelle ore immediatamente precedenti il prelievo, in quanto questi fattori sono in grado di modificare significativamente e in breve tempo i livelli dei TG. L’assunzione di alcool può aumentare i livelli di TG: per questo motivo,quando si intende verificare la presenza di una ipetrigliceridemia primitiva, l’alcool andrebbe sospeso nei giorni precedenti il prelievo. L’ora del prelievo riveste una particolare importanza in quanto la concentrazione dei TG varia in maniera considerevole durante il giorno anche indipendentemente dall’assunzione di cibo. Il prelievo dovrebbe pertanto essere effettuato nelle prime ore del mattino e dopo digiuno di 12 ore avendo peraltro mantenuto nei giorni precedenti il prelievo il regime dietetico abituale. Riguardo ai farmaci, quelli che possono modificare significativamente la concentrazione dei trigliceridi sono i diuretici, i beta bloccanti, e gli estrogeni (che provocano un aumento) e l’eparina e gli eparinoidi che potrebbero invece determinarne una diminuzione." In assenza del corpo del reato (il primo dei due campioni di siero) il caso può essere trattato solamente per via indiziaria. Anche se l’argomento (1) è significativo, ma può essere considerato un argomento debole, gli argomenti (2), (3) e (4) sono argomenti forti a favore dell’assenza di sbagli da parte del laboratorio. I risultati sono invece (argomento 5) compatibili con l’ampia variabilità biologica dell’analisi in questione, che risulta corroborata dei numerosissimi casi analoghi presenti nel database del laboratorio. Pertanto viene consigliata una accurata valutazione anamnestica del paziente per la possibile presenza di fattori preanalitici in grado di avere determinare la variabilità dei valori rilevata. ********************************
 Una volta scelto un valore soglia per separare i soggetti di un gruppo da quelli dell'altro gruppo, si trova che la maggior parte dei soggetti del primo gruppo (non immuni) viene classificato correttamente dal test diagnostico (sono i veri negativi = VN), e che la maggior parte dei soggetti del secondo gruppo (soggetti immuni) viene classificata correttamente dal test diagnostico (sono i veri positivi = VP). Tuttavia, a causa dei limiti inerenti a qualsasi tipo di test/classificazione, accade anche che qualche soggetto senza le IgG sia classificato dal test come soggetto che le ha (FP = falsi positivi), e per converso accade che qualche soggetto con le IgG sia classificato come soggetto che non le ha (FN = falsi negativi). In un recente lavoro [Maudry A, Chene G, Chatelain R, Patural H, Bellete B, Tisseur B, Hafid J, Raberin H, Beretta S, Tran Manh Sung R, Belot G, Flori P. Bicentric Evaluation of Six Anti-Toxoplasma Immunoglobulin G (IgG) Automated Immunoassays and Comparison to the Toxo II IgG Western Blot. Clinical and vaccine imunology, Sept. 2009, p. 1322–1326] sono stati presi in considerazione i principali test diagnostici di routine per la determinazione nel siero degli anticorpi anti-toxoplasma della classe IgG, confrontandoli con un test (immunoblotting) di secondo livello, più complesso e più costoso, ma ritenuto anche più accurato. I test diagnostici di routine hanno dimostrato di avere sensibilità e specificità eccellenti, come illustrato nelle tabella che segue. Ma non sono in grado di fornire la certezza assoluta (che si avrebbe solamente nel caso di un test con una sensibilità uguale al 100% e una specificità uguale al 100%: valori irraggiungibili nella pratica).
Una volta scelto un valore soglia per separare i soggetti di un gruppo da quelli dell'altro gruppo, si trova che la maggior parte dei soggetti del primo gruppo (non immuni) viene classificato correttamente dal test diagnostico (sono i veri negativi = VN), e che la maggior parte dei soggetti del secondo gruppo (soggetti immuni) viene classificata correttamente dal test diagnostico (sono i veri positivi = VP). Tuttavia, a causa dei limiti inerenti a qualsasi tipo di test/classificazione, accade anche che qualche soggetto senza le IgG sia classificato dal test come soggetto che le ha (FP = falsi positivi), e per converso accade che qualche soggetto con le IgG sia classificato come soggetto che non le ha (FN = falsi negativi). In un recente lavoro [Maudry A, Chene G, Chatelain R, Patural H, Bellete B, Tisseur B, Hafid J, Raberin H, Beretta S, Tran Manh Sung R, Belot G, Flori P. Bicentric Evaluation of Six Anti-Toxoplasma Immunoglobulin G (IgG) Automated Immunoassays and Comparison to the Toxo II IgG Western Blot. Clinical and vaccine imunology, Sept. 2009, p. 1322–1326] sono stati presi in considerazione i principali test diagnostici di routine per la determinazione nel siero degli anticorpi anti-toxoplasma della classe IgG, confrontandoli con un test (immunoblotting) di secondo livello, più complesso e più costoso, ma ritenuto anche più accurato. I test diagnostici di routine hanno dimostrato di avere sensibilità e specificità eccellenti, come illustrato nelle tabella che segue. Ma non sono in grado di fornire la certezza assoluta (che si avrebbe solamente nel caso di un test con una sensibilità uguale al 100% e una specificità uguale al 100%: valori irraggiungibili nella pratica).
 Una specificità inferiore al 100% comporta un valore predittivo del test positivo inferiore al 100%: questo significa che il test è positivo sia nei soggetti malati (nel caso specifico in tutti i soggetti malati, data la sensibilità del 100% del test) sia in alcuni soggetti sani. Sui soggetti risultati positivi al test di primo livello viene allora eseguito un test di secondo livello, più complesso e costoso, ma più specifico (per esempio un test diretto per la ricerca nel sangue dell’RNA del virus dell’epatite C). Il test di secondo livello consente di discriminare all’interno dei soggetti risultati positivi al test di primo livello i veri positivi (VP), cioè i soggetti con infezione da virus dell’epatite C, dai falsi positivi (FP), soggetti senza infezione ma nei quali il test di primo livello è risultato positivo: e non per un errore del laboratorio, ma semplicemente per i limiti intrinseci al test di primo livello, limiti derivanti dalla scelta di una soglia tra sani e malati che ha privilegiato la sensibilità, pagando per questo lo scotto sotto forma di una riduzione della specificità del test. Questo concetto lo trovate sviluppato nella parte dedicata a strategie diagnostiche e teorema di Bayes in particolare nel problema 7 della parte riservata agli esempi. Ho preparato una breve discussione sull'argomento anticorpi anti-HCV che risponde ai dubbi del paziente, e che mi pare utile e didattica. Le unità di misura della clearance della creatinina Un paziente ci ha chiesto un chiarimento in merito alle unità di misura nelle quali è espressa la clearance della creatinina. Rispondo con questo breve documento, dal titolo magari un pò ovvio, “Quali sono le unità di misura nelle quali espressa la clearance della creatinina?”, ma che consente di mettere a fuoco alcuni concetti della massima importanza, indispensabili anche per meglio comprendere le argomentazioni che stanno alla base del no alla presenza nel referto di laboratorio dell’eGFR, che gli (eventuali) interessati possono trovare al punto seguente. eGFR - Anatomia di una equazione Un paziente ci chiede se eseguiamo l’analisi denominata “eGFR”. Preciso subito che l’eGFR non è una analisi che viene eseguita “fisicamente” sul sangue del paziente. L’eGFR è il valore numerico che risulta dalla applicazione di una equazione matematica al risultato di un’altra analisi, questa invece comune e assai frequentemente eseguita: la determinazione della concentrazione della creatinina nel siero. Ma la domanda è molto, molto interessante. Premetto che come medico di laboratorio il mio dovere è contribuire ad estendere i sensi del medico/clinico con l’informazione derivante dallo studio dell’organismo in dimensioni che sfuggono all’osservazione diretta da parte del clinico nel suo rapporto con il paziente: fatto che rende significativa la piccolissima parte di medicina di mia competenza. Per fare questo mi sono sempre basato su metodo e principi della scienza: anche se scienza applicata, il laboratorio clinico è fatto di metodo e principi scientifici. E’ sulla base di questa idea fondamentale, sulla quale ho basato la mia vita professionale, che intervengo sul tema dell’eGFR, la “velocità di filtrazione glomerulare stimata”. L’argomento è complesso, tanto che ho dovuto svilupparlo in uno scritto a parte, che ho intitolato “eGFR (estimated Glomerular Filtration Rate) - Anatomia di una equazione. Ho quindi aggiunto un altro scritto, più conciso, semplificato dal punto di vista tecnico, e maggiormente orientato a illustrare le ragioni del no, dal titolo “’Dalla creatinina nel siero all’eGFR e ritorno. I perchè di un no alla presenza dell’eGFR nel referto di laboratorio”. Sono certo che entrambi aiuteranno il nostro paziente a comprendere perché, in attesa che la situazione si chiarisca dal punto di vista scientifico, nei referti del nostro laboratorio non compare l’eGFR. Test di laboratorio per l’influenza (di tipo A e di tipo B) Un paziente ci chiede per quale ragione abbiamo deciso di non eseguire nel nostro laboratorio il test per l’influenza (test per l’infezione da virus dell’influenza di tipo A [che include il virus definito come A(H1N1)v] e di tipo B). Innanzitutto va premesso che per la diagnosi di infezione da virus influenzali esistono vari tipi di test, ma che solamente un tipo di test, che fornisce una “ragionevole presunzione” di infezione, denominato “test rapido”, è alla portata dei comuni laboratori di analisi cliniche. I test che forniscono la “certezza” di infezione prevedono la coltura dei virus su cellule umane e, sia per la sicurezza degli operatori sia (e questa è la ragione principale) per la tutela della salute pubblica (per evitare fughe di virus con i potenziali danni conseguenti sulla popolazione), sono richieste condizioni operative così stringenti che (per esempio) in Italia solamente tre laboratori sono in grado di assicurare questi test, che chiamiamo “test di riferimento”. Dato che la tutela della salute pubblica è uno degli interessi principali dello Stato, tutti i governi (anche quelli che non hanno un sistema sanitario pubblico) hanno messo a disposizione dei cittadini informazioni assolutamente aggiornate in merito, e sul web potete trovare una quantità quasi illimitata di informazioni scientificamente corrette da fonti attendibili (si tratta solo di saperle selezionare). Ma la domanda è oltremodo interessante, perchè mi consente di appellarmi al contenuto del mio sito www.bayes.it che, tra premesse, formule, esempi e programmi, ho dedicato quasi per metà al teorema di Bayes. Che anche nel caso dell’influenza riveste un ruolo esplicativo centrale: vediamo come, partendo dalla citazione di due (tra i tanti) lavori che lo utilizzano/ne utilizzano i presupposti. Nel lavoro “C.K.Y. Cheng et al. / Factors affecting QuickVue Influenza A + B rapid test performance in the community setting / Diagnostic Microbiology and Infectious Disease 65 (2009) 35–41” si afferma che “i test rapidi hanno una sensibilità di 0.68 e una specificità di 0.96 quando confrontati con la coltura del virus”. Nel lavoro “C. Ruef / Diagnosing Influenza – Clinical Assessment and/or Rapid Antigen Testing? / Infection 2007; 35: 49–50” si afferma che la diagnosi di influenza basata sui segni clinici [insorgenza acuta, febbre elevata e tosse secca] ha una “sensibilità del 33% e specificità del 98%.” Sono queste due affermazioni sufficienti per trarre una qualche conclusione? Direi proprio di si. Guardate le due seguenti tabelle, ottenute mediante il mio semplicissimo programma per il calcolo del valore predittivo di un test di laboratorio a partire da sensibilità, specificità e prevalenza, utilizzando il teorema di Bayes. Impiegando i valori di sensibilità (0,68) e di specificità (0,96) dei test rapidi indicati da Cheng si ottengono, in funzione dei valori della prevalenza della malattia “influenza” che vanno dal 5 per mille (0,005) al 20% (0,20), il valore predittivo di un test positivo (VPT+) e il valore predittivo di un test negativo (VPT-) che trovate qui nelle due colonne di destra:
Una specificità inferiore al 100% comporta un valore predittivo del test positivo inferiore al 100%: questo significa che il test è positivo sia nei soggetti malati (nel caso specifico in tutti i soggetti malati, data la sensibilità del 100% del test) sia in alcuni soggetti sani. Sui soggetti risultati positivi al test di primo livello viene allora eseguito un test di secondo livello, più complesso e costoso, ma più specifico (per esempio un test diretto per la ricerca nel sangue dell’RNA del virus dell’epatite C). Il test di secondo livello consente di discriminare all’interno dei soggetti risultati positivi al test di primo livello i veri positivi (VP), cioè i soggetti con infezione da virus dell’epatite C, dai falsi positivi (FP), soggetti senza infezione ma nei quali il test di primo livello è risultato positivo: e non per un errore del laboratorio, ma semplicemente per i limiti intrinseci al test di primo livello, limiti derivanti dalla scelta di una soglia tra sani e malati che ha privilegiato la sensibilità, pagando per questo lo scotto sotto forma di una riduzione della specificità del test. Questo concetto lo trovate sviluppato nella parte dedicata a strategie diagnostiche e teorema di Bayes in particolare nel problema 7 della parte riservata agli esempi. Ho preparato una breve discussione sull'argomento anticorpi anti-HCV che risponde ai dubbi del paziente, e che mi pare utile e didattica. Le unità di misura della clearance della creatinina Un paziente ci ha chiesto un chiarimento in merito alle unità di misura nelle quali è espressa la clearance della creatinina. Rispondo con questo breve documento, dal titolo magari un pò ovvio, “Quali sono le unità di misura nelle quali espressa la clearance della creatinina?”, ma che consente di mettere a fuoco alcuni concetti della massima importanza, indispensabili anche per meglio comprendere le argomentazioni che stanno alla base del no alla presenza nel referto di laboratorio dell’eGFR, che gli (eventuali) interessati possono trovare al punto seguente. eGFR - Anatomia di una equazione Un paziente ci chiede se eseguiamo l’analisi denominata “eGFR”. Preciso subito che l’eGFR non è una analisi che viene eseguita “fisicamente” sul sangue del paziente. L’eGFR è il valore numerico che risulta dalla applicazione di una equazione matematica al risultato di un’altra analisi, questa invece comune e assai frequentemente eseguita: la determinazione della concentrazione della creatinina nel siero. Ma la domanda è molto, molto interessante. Premetto che come medico di laboratorio il mio dovere è contribuire ad estendere i sensi del medico/clinico con l’informazione derivante dallo studio dell’organismo in dimensioni che sfuggono all’osservazione diretta da parte del clinico nel suo rapporto con il paziente: fatto che rende significativa la piccolissima parte di medicina di mia competenza. Per fare questo mi sono sempre basato su metodo e principi della scienza: anche se scienza applicata, il laboratorio clinico è fatto di metodo e principi scientifici. E’ sulla base di questa idea fondamentale, sulla quale ho basato la mia vita professionale, che intervengo sul tema dell’eGFR, la “velocità di filtrazione glomerulare stimata”. L’argomento è complesso, tanto che ho dovuto svilupparlo in uno scritto a parte, che ho intitolato “eGFR (estimated Glomerular Filtration Rate) - Anatomia di una equazione. Ho quindi aggiunto un altro scritto, più conciso, semplificato dal punto di vista tecnico, e maggiormente orientato a illustrare le ragioni del no, dal titolo “’Dalla creatinina nel siero all’eGFR e ritorno. I perchè di un no alla presenza dell’eGFR nel referto di laboratorio”. Sono certo che entrambi aiuteranno il nostro paziente a comprendere perché, in attesa che la situazione si chiarisca dal punto di vista scientifico, nei referti del nostro laboratorio non compare l’eGFR. Test di laboratorio per l’influenza (di tipo A e di tipo B) Un paziente ci chiede per quale ragione abbiamo deciso di non eseguire nel nostro laboratorio il test per l’influenza (test per l’infezione da virus dell’influenza di tipo A [che include il virus definito come A(H1N1)v] e di tipo B). Innanzitutto va premesso che per la diagnosi di infezione da virus influenzali esistono vari tipi di test, ma che solamente un tipo di test, che fornisce una “ragionevole presunzione” di infezione, denominato “test rapido”, è alla portata dei comuni laboratori di analisi cliniche. I test che forniscono la “certezza” di infezione prevedono la coltura dei virus su cellule umane e, sia per la sicurezza degli operatori sia (e questa è la ragione principale) per la tutela della salute pubblica (per evitare fughe di virus con i potenziali danni conseguenti sulla popolazione), sono richieste condizioni operative così stringenti che (per esempio) in Italia solamente tre laboratori sono in grado di assicurare questi test, che chiamiamo “test di riferimento”. Dato che la tutela della salute pubblica è uno degli interessi principali dello Stato, tutti i governi (anche quelli che non hanno un sistema sanitario pubblico) hanno messo a disposizione dei cittadini informazioni assolutamente aggiornate in merito, e sul web potete trovare una quantità quasi illimitata di informazioni scientificamente corrette da fonti attendibili (si tratta solo di saperle selezionare). Ma la domanda è oltremodo interessante, perchè mi consente di appellarmi al contenuto del mio sito www.bayes.it che, tra premesse, formule, esempi e programmi, ho dedicato quasi per metà al teorema di Bayes. Che anche nel caso dell’influenza riveste un ruolo esplicativo centrale: vediamo come, partendo dalla citazione di due (tra i tanti) lavori che lo utilizzano/ne utilizzano i presupposti. Nel lavoro “C.K.Y. Cheng et al. / Factors affecting QuickVue Influenza A + B rapid test performance in the community setting / Diagnostic Microbiology and Infectious Disease 65 (2009) 35–41” si afferma che “i test rapidi hanno una sensibilità di 0.68 e una specificità di 0.96 quando confrontati con la coltura del virus”. Nel lavoro “C. Ruef / Diagnosing Influenza – Clinical Assessment and/or Rapid Antigen Testing? / Infection 2007; 35: 49–50” si afferma che la diagnosi di influenza basata sui segni clinici [insorgenza acuta, febbre elevata e tosse secca] ha una “sensibilità del 33% e specificità del 98%.” Sono queste due affermazioni sufficienti per trarre una qualche conclusione? Direi proprio di si. Guardate le due seguenti tabelle, ottenute mediante il mio semplicissimo programma per il calcolo del valore predittivo di un test di laboratorio a partire da sensibilità, specificità e prevalenza, utilizzando il teorema di Bayes. Impiegando i valori di sensibilità (0,68) e di specificità (0,96) dei test rapidi indicati da Cheng si ottengono, in funzione dei valori della prevalenza della malattia “influenza” che vanno dal 5 per mille (0,005) al 20% (0,20), il valore predittivo di un test positivo (VPT+) e il valore predittivo di un test negativo (VPT-) che trovate qui nelle due colonne di destra:
|
|
|
|
|
|
|
|
Ultimo aggiornamento: 20 febbraio 2023
NOTA SUI COLLEGAMENTIALLE FONTI BIBLIOGRAFICHE La maggior parte dei collegamenti ad articoli scientifici riportati nel sito fa riferimento a riviste online che forniscono gratuitamente l’articolo originale. In alcuni casi è necessario registrarsi sul sito per avere libero accesso agli articoli: questo accade per esempio con il BMJ. Quando i collegamenti fanno riferimento a fonti bibliografiche a pagamento, chi non ha sottoscritto un abbonamento con la rivista potrebbe vedere comparire un messaggio del tipo “access forbidden”, ma il più delle volte vedrà comparire una pagina che consente di acquistare online l’articolo originale.
Programma di statistica Ministat (versione per Windows)

Programma di statistica Open Source R(per Linux, Mac OS X e Windows)
Manuale Merck di diagnosie terapia
L’articolo da non perdere...
Errori congeniti del metabolismo
I migliori libri del mese Leonard Mlodinow La passeggiata dell’ubriaco. Le leggi scientifiche del caso.Rizzoli Editore, 2009, pp. 294ISBN: 17034081
OpenOffice, la suite Open Source (per Linux, Mac OS X e Windows)
ebooks... Mauss, Berg, Rockstroh, Sarrazin, Wedemeyer.Hepatology - A clinical textbook. 10th Edition - 2020
Le lettureconsigliate
Atlante di anatomia del Bock
Tavole metaboliche
Informazioni: info@bayes.itScrivimi: webmaster@bayes.it
NOTA LEGALE L’interpretazione dei risultati delle analisi di laboratorio deve essere effettuata esclusivamente dal medico e alla luce dei dati clinici.Questo sito ha uno scopo esclusivamente educativo e formativo. Pertanto le informazioni in esso contenute possono essere utilizzate esclusivamente a scopo didattico, e anche in questo caso sotto la responsabilità personale di chi le utilizza, sia per sé stesso sia per terzi.Le informazioni contenute in questo sito non possono e non devono essere utilizzate né a scopo diagnostico, né a scopo prognostico, né a scopo terapeutico, né per qualsiasi attività che abbia un impatto sia diretto sia indiretto sullo stato di salute di un individuo o di più individui.Nessuna responsabilità può essere imputata all’autore per danni diretti o indiretti e di qualsivoglia natura che potrebbero essere causati a sé stessi o a terzi a causa di errori, imprecisioni, omissioni, interpretazioni o utilizzo dei contenuti di questo sito o dei siti cui esso fa riferimento.
E ora che i test genetici sono alla portata di tutti?Con meno di mille euro è possibile comprare un test genetico su Internet: si manda un piccolo campione di cellule e poi si aspetta la risposta. Ma... a che cosa serve la risposta? Un dossier di Marika De Acetis dall’Archivio storico del sito www.torinoscienza.it
[Home] [Errori cognitivi] [Epistemologia] [Teorema di Bayes] [Decisioni mediche] [Le basi biochimiche][Analisi tradizionali] [Analisi genetiche] [Qualità in laboratorio] [Statistica e laboratorio][Storia delle medicina] [Download] [Link] [Bacheca] [FAQ] [Chi sono]
Attualità in tema di eGFR:
I migliori libri del mese Giovanni Federspil Logica clinica. I principi del metodo in medicina.McGraw-Hill, 2004, pp. 368ISBN: 88 386 2984-6
Atlante di virologia
Dal settembre 2008oltre 400 000 visitatori
ebooks... M. BesozziErrori cognitivi, probabilità e decisioni mediche. Fate click sul titolo o scaricate il testo su tablet o smartphone con il codice a barre riportato qui sotto. 

Atlante dei protozoi intestinali
Atlante di citologia e istologia
Statistica e grafica con R
Espressione dei risultati nel laboratorio di chimica clinica
Pathology outlines
Atlante di anatomia del Gray
Atlante di ematologia
Atlante di parassitologia
Micobatteriologia clinica
Concetti, metodi e strumenti per una
buona informazione
ebooks... M. BesozziStatistica e grafica con R Fate click sul titolo o scaricate il testo su tablet o smartphone con il codice a barre riportato qui sotto. 

I migliori libri del mese Luigi Tesio I bravi e i buoni.Perché la medicina clinica può essere una scienza.Il Pensiero Scientifico Editore, 2015, pp. 216 ISBN: 978-88-490-0538-7
Gli inganni della correlazione:
Storia delle unità di misura
Questo sito è stato archiviato ed è reso disponibile esclusivamente come memoria storica: pertanto è escluso ogni suo possibile utilizzo medico. Le parti del sito riservate al teorema di Bayes rimangono concettualmente valide, ma declino qualsiasi responsabilità per la lenta ma inevitabile obsolescenza dei restanti contenuti dovuta alla comparsa di nuove analisi di laboratorio, di progressi nelle analisi genetiche, di link interrotti, e quant’altro.
.